如果你也在 怎样代写热力学Thermodynamics 这个学科遇到相关的难题,请随时右上角联系我们的24/7代写客服。热力学Thermodynamics是物理学的一个分支,涉及热、功和温度,以及它们与能量、熵以及物质和辐射的物理特性的关系。这些数量的行为受热力学四大定律的制约,这些定律使用可测量的宏观物理量来传达定量描述,但可以用统计力学的微观成分来解释。热力学适用于科学和工程中的各种主题,特别是物理化学、生物化学、化学工程和机械工程,但也适用于其他复杂领域,如气象学。
热力学Thermodynamics从历史上看,热力学的发展源于提高早期蒸汽机效率的愿望,特别是通过法国物理学家萨迪-卡诺(1824年)的工作,他认为发动机的效率是可以帮助法国赢得拿破仑战争的关键。苏格兰-爱尔兰物理学家开尔文勋爵在1854年首次提出了热力学的简明定义,其中指出:”热力学是关于热与作用在身体相邻部分之间的力的关系,以及热与电的关系的课题。” 鲁道夫-克劳修斯重述了被称为卡诺循环的卡诺原理,为热学理论提供了更真实、更健全的基础。他最重要的论文《论热的运动力》发表于1850年,首次提出了热力学的第二定律。1865年,他提出了熵的概念。1870年,他提出了适用于热的维拉尔定理。
热力学Thermodynamics代写,免费提交作业要求, 满意后付款,成绩80\%以下全额退款,安全省心无顾虑。专业硕 博写手团队,所有订单可靠准时,保证 100% 原创。最高质量的热力学Thermodynamics作业代写,服务覆盖北美、欧洲、澳洲等 国家。 在代写价格方面,考虑到同学们的经济条件,在保障代写质量的前提下,我们为客户提供最合理的价格。 由于作业种类很多,同时其中的大部分作业在字数上都没有具体要求,因此热力学Thermodynamics作业代写的价格不固定。通常在专家查看完作业要求之后会给出报价。作业难度和截止日期对价格也有很大的影响。
同学们在留学期间,都对各式各样的作业考试很是头疼,如果你无从下手,不如考虑my-assignmentexpert™!
my-assignmentexpert™提供最专业的一站式服务:Essay代写,Dissertation代写,Assignment代写,Paper代写,Proposal代写,Proposal代写,Literature Review代写,Online Course,Exam代考等等。my-assignmentexpert™专注为留学生提供Essay代写服务,拥有各个专业的博硕教师团队帮您代写,免费修改及辅导,保证成果完成的效率和质量。同时有多家检测平台帐号,包括Turnitin高级账户,检测论文不会留痕,写好后检测修改,放心可靠,经得起任何考验!
想知道您作业确定的价格吗? 免费下单以相关学科的专家能了解具体的要求之后在1-3个小时就提出价格。专家的 报价比上列的价格能便宜好几倍。
物理代写|热力学代写Thermodynamics代考|Working with constant temperature
Heating and cooling an ideal gas at a constant temperature is kind of tricky. If you allow a high-pressure gas to expand in a piston-cylinder to produce work, the gas temperature will decrease. You can maintain a constant temperature in the gas by adding just the right amount of heat to it during the expansion process. The Stirling cycle and the Ericsson cycle (see Chapter 18) have isothermal compression and expansion processes.
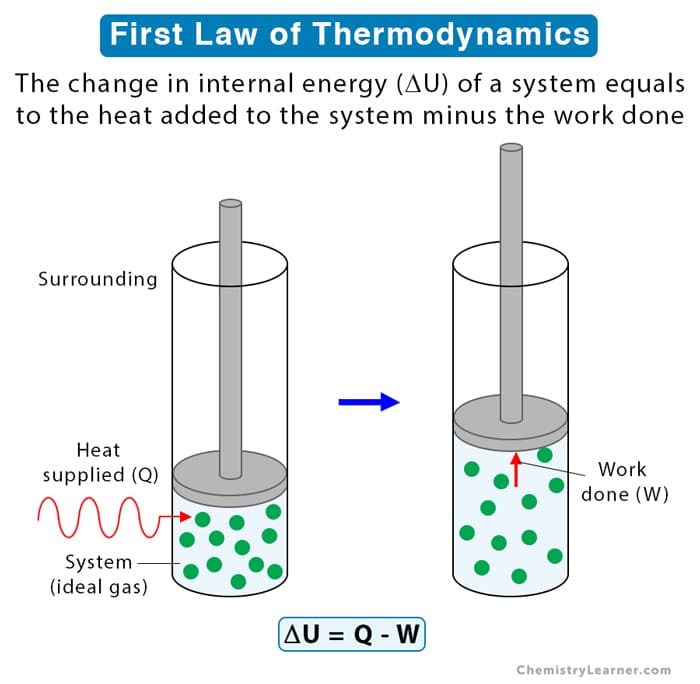
In an isothermal process with an ideal gas, the internal energy in the system doesn’t change because the initial and final temperatures are the same. Because $\Delta U$ equals zero, the energy equation simplifies to $Q=W$.
You calculate the work done by a piston in a closed system for an isothermal process using the following equation, introduced in Chapter 4:
$$
W=P_1 V_1 \ln \frac{V_2}{V_1}
$$
The ideal-gas law is used to determine the pressure and volume relationship between the initial and final states of a constant-temperature process. Because the temperature is constant, the ideal-gas law relationship reduces to
$$
\frac{P_1 V_1}{T_1}=\frac{P_2 V_2}{T_2}
$$
or
$$
P_1 V_1=P_2 V_2
$$
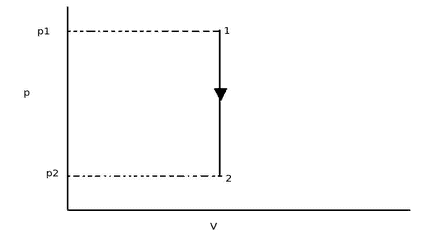
A cylinder starts with a volume of 0.1 liter at 3,000 kilopascals and 25 degrees Celsius. The gas expands until the volume is 1.0 liter. Heat is added to the cylinder to keep the gas at 25 degrees Celsius. During the process, the pressure inside the cylinder decreases. Figure 5 -3 shows this process as the thick arrow from States 1 to 2 on the $P-v$ diagram on the right side of the figure. The area under the $P-v$ curve is the amount of work in the process.
物理代写|热力学代写Thermodynamics代考|working with an adiabatic process
In previous sections, I set $W$ or $\Delta U$ to zero in the energy equation for different thermodynamic processes. Now it’s time for $Q$ to be zero. When heat doesn’t enter or leave a system, the process is adiabatic. The energy equation for a closed system simplifies to this result for an ideal gas:
$$
W=-\Delta U=m\left(u_1-u_2\right)=m \cdot c_e\left(T_1-T_2\right)
$$
You calculate the work done by a frictionless piston in a closed system for a reversible and adiabatic process using the following equation, introduced in Chapter 4. A process is reversible if both the system and the surroundings return to their initial state when the process proceeds in the reverse direction. The following equation assumes the specific heat is constant during the process. You can have better accuracy in calculating the work if you use the specific heats of the gas at the average process temperature.
$$
W=\frac{P_2 V_2-P_1 V_1}{1-k}
$$
In this equation, $k$ is the ratio of constant-pressure $\left(c_p\right)$ and the constantvolume $\left(c_e\right)$ specific heat of the gas:
$$
k=\frac{c_p}{c_p}
$$
For air around room temperature, $k$ equals 1.4. The value of $k$ changes with temperature. You can look up the specific heat of air at different temperatures in Table A-1 of the appendix to calculate the value of $k$ at different temperatures. You find the constant-volume specific heat $\left(c_p\right)$ using the constantpressure specific heat $\left(c_p\right)$ and the gas constant $(R)$ in this equation:
$$
c_e=c_p-R
$$
The ideal-gas law is used to determine the $P-v-T$ relationships between States 1 and 2 for a process. For a reversible, adiabatic process, $P-v-T$ relationships are written in several ways, as shown here:
$$
\frac{P_2}{P_1}=\left(\frac{V_1}{V_2}\right)^k \text { or } \frac{T_2}{T_1}=\left(\frac{V_1}{V_2}\right)^{n-1}=\left(\frac{P_2}{P_1}\right)^{(k-1) / k}
$$
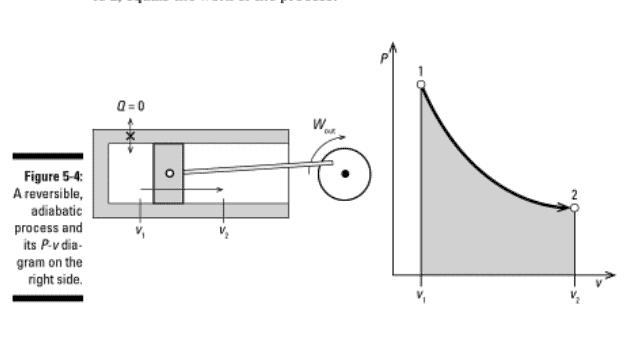
The cylinder shown in Figure 5-4 is insulated so that no heat can enter or leave it. The cylinder starts with a volume of 0.1 liter at 3,000 kilopascals and 25 degrees Celsius. The gas expands until the volume inside the cylinder is 1 liter. The right side of Figure $5-4$ shows the process on a $P-v$ diagram. The area under the $P-v$ curve, shown by the thick line with an arrow from States 1 to 2 , equals the work of the process.
热力学代写
物理代写|热力学代写Thermodynamics代考|Working with constant temperature
在恒定温度下加热和冷却理想气体有点棘手。如果让高压气体在活塞缸中膨胀做功,气体温度就会降低。你可以通过在膨胀过程中加入适量的热量来保持气体的恒定温度。斯特林旋回和埃里克森旋回(见第18章)具有等温压缩和膨胀过程。
在理想气体等温过程中,由于初始温度和最终温度相同,系统的内能不发生变化。因为$\Delta U$等于零,能量方程简化为$Q=W$ .
你可以用下面的公式计算一个活塞在一个封闭系统中对等温过程所做的功,在第4章中介绍:
$$
W=P_1 V_1 \ln \frac{V_2}{V_1}
$$
理想气体定律用于确定一个恒温过程的初始状态和最终状态之间的压力和体积关系。因为温度是恒定的,理想气体定律的关系减小到
$$
\frac{P_1 V_1}{T_1}=\frac{P_2 V_2}{T_2}
$$
或
$$
P_1 V_1=P_2 V_2
$$
一个圆柱体在3000千帕和25摄氏度的温度下,体积为0.1升。气体膨胀到体积为1.0升。将热量加到钢瓶中,使气体保持在25摄氏度。在此过程中,气缸内的压力减小。图5 -3显示了这个过程,如图右侧$P-v$图中从状态1到状态2的粗箭头所示。$P-v$曲线下的面积是这个过程中的功。
物理代写|热力学代写Thermodynamics代考|working with an adiabatic process
在前面的章节中,我将不同热力学过程的能量方程中的$W$或$\Delta U$设为零。现在是时候将$Q$归零了。当热量不进入或离开系统时,这个过程是绝热的。封闭系统的能量方程简化为理想气体的结果:
$$
W=-\Delta U=m\left(u_1-u_2\right)=m \cdot c_e\left(T_1-T_2\right)
$$
你可以用下面的公式计算封闭系统中一个可逆绝热过程的无摩擦活塞所做的功,这在第4章中介绍过。如果过程向相反方向进行时,系统和环境都恢复到初始状态,则过程是可逆的。下式假设在此过程中比热是恒定的。如果用平均工艺温度下气体的比热来计算功,就会比较准确。
$$
W=\frac{P_2 V_2-P_1 V_1}{1-k}
$$
式中$k$为气体定压$\left(c_p\right)$与定容$\left(c_e\right)$比热之比:
$$
k=\frac{c_p}{c_p}
$$
对于室温左右的空气,$k$ = 1.4。$k$值随温度变化。可参考附录表A-1中不同温度下的空气比热,计算不同温度下$k$的值。你用定压比热$\left(c_p\right)$和气体常数$(R)$在这个方程中找到定容比热$\left(c_p\right)$:
$$
c_e=c_p-R
$$
理想气体定律用于确定过程状态1和状态2之间的$P-v-T$关系。对于一个可逆的绝热过程,$P-v-T$关系可以用几种方式表示,如下所示:
$$
\frac{P_2}{P_1}=\left(\frac{V_1}{V_2}\right)^k \text { or } \frac{T_2}{T_1}=\left(\frac{V_1}{V_2}\right)^{n-1}=\left(\frac{P_2}{P_1}\right)^{(k-1) / k}
$$
图5-4所示的气缸是隔热的,因此没有热量可以进入或离开它。在3000千帕斯卡和25摄氏度的温度下,圆柱体的体积为0.1升。气体膨胀到气缸内的体积为1升。图$5-4$的右侧显示了$P-v$图上的过程。$P-v$曲线下的面积,用从状态1到状态2的粗线和箭头表示,等于这个过程的功。

物理代写|热力学代写Thermodynamics代考 请认准UprivateTA™. UprivateTA™为您的留学生涯保驾护航。
微观经济学代写
微观经济学是主流经济学的一个分支,研究个人和企业在做出有关稀缺资源分配的决策时的行为以及这些个人和企业之间的相互作用。my-assignmentexpert™ 为您的留学生涯保驾护航 在数学Mathematics作业代写方面已经树立了自己的口碑, 保证靠谱, 高质且原创的数学Mathematics代写服务。我们的专家在图论代写Graph Theory代写方面经验极为丰富,各种图论代写Graph Theory相关的作业也就用不着 说。
线性代数代写
线性代数是数学的一个分支,涉及线性方程,如:线性图,如:以及它们在向量空间和通过矩阵的表示。线性代数是几乎所有数学领域的核心。
博弈论代写
现代博弈论始于约翰-冯-诺伊曼(John von Neumann)提出的两人零和博弈中的混合策略均衡的观点及其证明。冯-诺依曼的原始证明使用了关于连续映射到紧凑凸集的布劳威尔定点定理,这成为博弈论和数学经济学的标准方法。在他的论文之后,1944年,他与奥斯卡-莫根斯特恩(Oskar Morgenstern)共同撰写了《游戏和经济行为理论》一书,该书考虑了几个参与者的合作游戏。这本书的第二版提供了预期效用的公理理论,使数理统计学家和经济学家能够处理不确定性下的决策。
微积分代写
微积分,最初被称为无穷小微积分或 “无穷小的微积分”,是对连续变化的数学研究,就像几何学是对形状的研究,而代数是对算术运算的概括研究一样。
它有两个主要分支,微分和积分;微分涉及瞬时变化率和曲线的斜率,而积分涉及数量的累积,以及曲线下或曲线之间的面积。这两个分支通过微积分的基本定理相互联系,它们利用了无限序列和无限级数收敛到一个明确定义的极限的基本概念 。
计量经济学代写
什么是计量经济学?
计量经济学是统计学和数学模型的定量应用,使用数据来发展理论或测试经济学中的现有假设,并根据历史数据预测未来趋势。它对现实世界的数据进行统计试验,然后将结果与被测试的理论进行比较和对比。
根据你是对测试现有理论感兴趣,还是对利用现有数据在这些观察的基础上提出新的假设感兴趣,计量经济学可以细分为两大类:理论和应用。那些经常从事这种实践的人通常被称为计量经济学家。
Matlab代写
MATLAB 是一种用于技术计算的高性能语言。它将计算、可视化和编程集成在一个易于使用的环境中,其中问题和解决方案以熟悉的数学符号表示。典型用途包括:数学和计算算法开发建模、仿真和原型制作数据分析、探索和可视化科学和工程图形应用程序开发,包括图形用户界面构建MATLAB 是一个交互式系统,其基本数据元素是一个不需要维度的数组。这使您可以解决许多技术计算问题,尤其是那些具有矩阵和向量公式的问题,而只需用 C 或 Fortran 等标量非交互式语言编写程序所需的时间的一小部分。MATLAB 名称代表矩阵实验室。MATLAB 最初的编写目的是提供对由 LINPACK 和 EISPACK 项目开发的矩阵软件的轻松访问,这两个项目共同代表了矩阵计算软件的最新技术。MATLAB 经过多年的发展,得到了许多用户的投入。在大学环境中,它是数学、工程和科学入门和高级课程的标准教学工具。在工业领域,MATLAB 是高效研究、开发和分析的首选工具。MATLAB 具有一系列称为工具箱的特定于应用程序的解决方案。对于大多数 MATLAB 用户来说非常重要,工具箱允许您学习和应用专业技术。工具箱是 MATLAB 函数(M 文件)的综合集合,可扩展 MATLAB 环境以解决特定类别的问题。可用工具箱的领域包括信号处理、控制系统、神经网络、模糊逻辑、小波、仿真等。